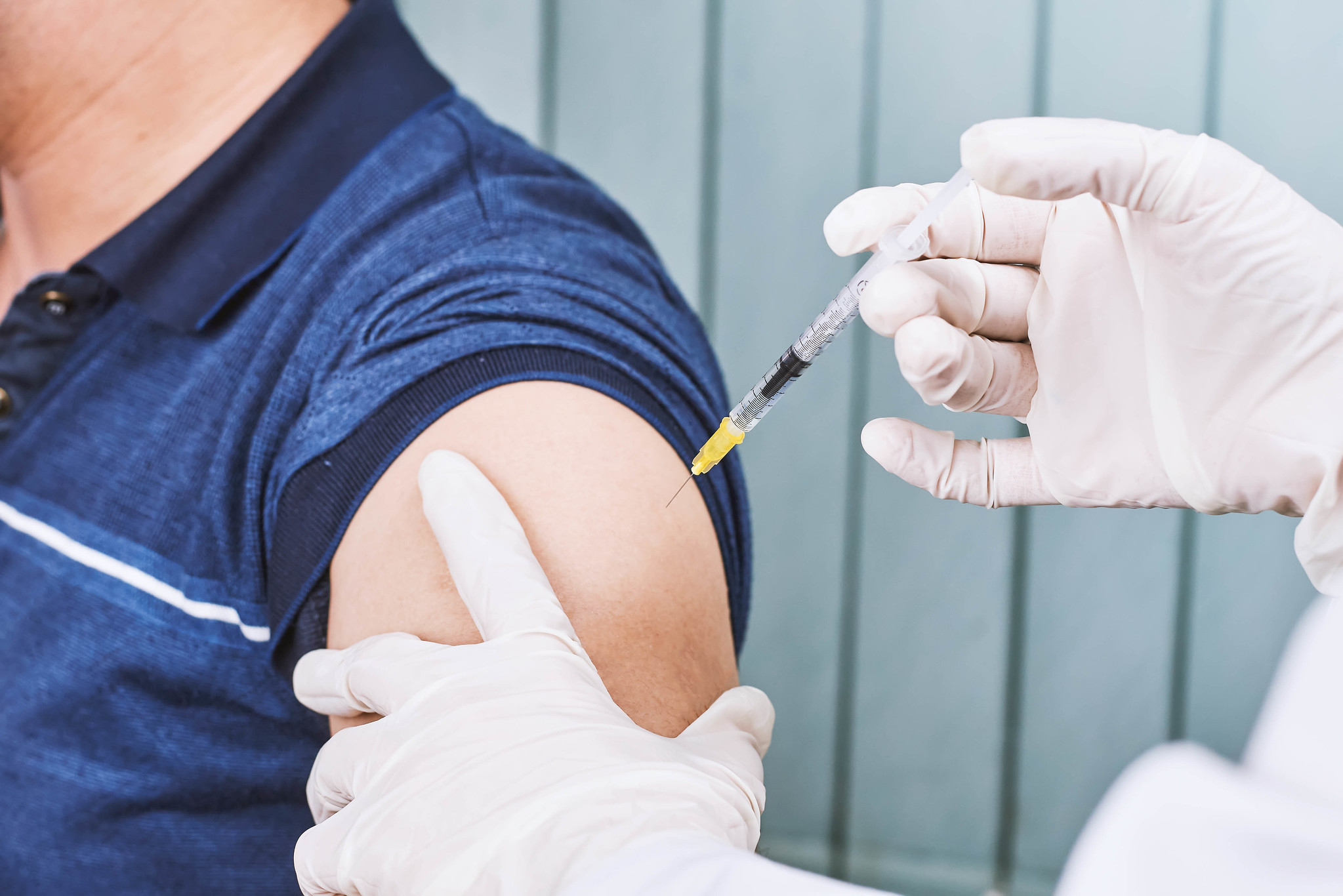
Aby powstrzymać pandemię COVID-19, pilnie potrzebne są skuteczne szczepionki. Kandydatką na kolejną taką szczepionkę jest Ad26.COV2.S, znana też jako szczepionka firmy Johnson & Johnson (lub firmy Janssen, gdyż Janssen Pharmaceutica stała się w roku 1961 częścią globalnego koncernu Johnson & Johnson).
Szczepionkę opracowały firma Janssen Pharmaceutica oraz specjaliści z Beth Israel Deaconess Medical Center (BIDMC).
Wykorzystuje ona tę samą technologię co wcześniej opracowana przez ten zespół i zatwierdzona przez Europejską Agencję Leków szczepionka przeciwko wirusowi ebola oraz będące w fazie badań szczepionki przeciwko syncytialnemu wirusowi oddechowemu (RSV), wirusom HIV i zika. Są to szczepionki na bazie niezdolnego do replikacji adenowirusa Ad26, uważane za ogólnie bezpieczne i wysoce immunogenne.
Ad26 jest nośnikiem materiału genetycznego, pod wpływem którego komórki zaszczepionej osoby zaczynają wytwarzać białko wypustkowe (białko kolca, białko S) wirusa SARS-CoV-2 powodującego COVID-19. Reagując na białko wirusa, organizm wytwarza odporność. Samo białko nie jest wirusem SARS-CoV-2, nie może więc spowodować choroby.
W odróżnieniu od trzech dotychczasowych szczepionek przeciwko COVID-19 (Pfizer, Moderna i AstraZeneca) w przypadku szczepionki Johnson & Johnson do uzyskania odporności powinna wystarczyć pojedyncza dawka. Co więcej, wstępne wyniki wskazywały na praktycznie 100-proc. skuteczność. Nie musi też być przechowywana w zamrażarce - można ją trzymać w zwykłej lodówce.
W rozpoczętym 22 lipca 2020 wieloośrodkowym (12 ośrodków w Belgii i USA), kontrolowanym placebo badaniu fazy 1–2a z podwójnie ślepą próbą losowo przydzielono zdrowych dorosłych w wieku od 18 do 55 lat (kohorta 1) oraz osoby w wieku 65 lat lub starsze (kohorta 3), którzy otrzymali domięśniowo szczepionkę Ad26.COV2.S w małej lub wysokiej dawce albo placebo. Część badanych otrzymała jedną dawkę, inni - dwie dawki w odstępie 56 dni. W kohorcie 2 zbierane są długoterminowe dane porównujące schemat pojedynczej dawki ze schematem dwudawkowym; wyniki te nie zostały na razie podane.
Po podaniu pierwszej dawki szczepionki 805 uczestnikom w kohortach 1 i 3 oraz po drugiej dawce w kohorcie 1, najczęściej zgłaszanymi działaniami niepożądanymi były zmęczenie, bóle głowy, bóle mięśni i bóle w miejscu wstrzyknięcia. Najczęstszym ogólnoustrojowym działaniem niepożądanym była gorączka. Ogólnoustrojowe zdarzenia niepożądane występowały rzadziej w kohorcie 3 niż w kohorcie 1 oraz u osób, które otrzymały małą dawkę szczepionki, niż u osób, które otrzymały dużą dawkę. Reaktogenność (odpowiedź na szczepienie) była mniejsza po drugiej dawce - podają autorzy badań, opublikowanych w "New England Journal of Medicine".
Miejscowe i ogólnoustrojowe reakcje wystąpiły w dniu szczepienia lub następnego dnia i na ogół ustępowały w ciągu 24 godzin. Reakcje ogólnoustrojowe były bardzo podatne na leki przeciwgorączkowe i nie stwierdzono potrzeby ich profilaktycznego stosowania. Po podaniu drugiej dawki wśród uczestników w wieku od 18 do 55 lat, częstość występowania ogólnoustrojowych poważnych działań niepożądanych była znacznie niższa niż po pierwszej immunizacji zarówno w grupie otrzymującej małą, jak i dużą dawkę.
Przeciwciała neutralizujące przeciwko wirusowi wykryto u 90 proc. lub więcej wszystkich uczestników 29 dnia po pierwszej dawce szczepionki, niezależnie od dawki lub grupy wiekowej i osiągnięto 100 proc. do dnia 57. W ciągu 71 dni obserwacji po podaniu pierwszej dawki miana przeciwciał wzrastały i stabilizowały się, co sugeruje trwałość odpowiedzi immunologicznej wywołanej przez Ad26.COV2.S.
Na obecnym etapie badań analiza wykazała, że szczepionka Ad26.COV2.S miała akceptowalny profil bezpieczeństwa i reaktogenności oraz wytwarzała odporność już po pojedynczym szczepieniu niską lub wysoką dawką. Trwają badania 3. fazy.
Chociaż we wszystkich trwających badaniach fazy 3 innych szczepionek przeciwko COVID-19 oceniano schematy dwudawkowe, pojedyncza dawka Ad26.COV2.S wywołała silną odpowiedź humoralną u większości zaszczepionych, z obecnością przeciwciał wiążących i neutralizujących białko S u ponad 90 proc. uczestników, niezależnie od grupy wiekowej lub dawki szczepionki.
Silne działanie Ad26.COV2.S potwierdzają wyniki badania z udziałem małp, w których pojedyncza dawka zapewniła całkowitą ochronę przed replikacją SARS-CoV-2 w płucach i prawie całkowitą ochronę w nosie.
Obecnie - w 3 fazie klinicznej - badane jest, czy druga dawka przyniesie dodatkowe korzyści w postaci poprawy skuteczności uodpornienia lub jego trwałości - zwłaszcza u osób starszych, których odpowiedź immunologiczna po pierwszej dawce była mniejsza niż u młodszych uczestników.